ایمنولوژی لنفویید فلیکول ها :
وجود فولیکول های حامل سلول های B در بیماران COPD های شدید دیده می شوند. هر چقدر که COPD شدیدتر می شود تعداد این فولیکول ها بیشتر می شود. این فولیکول ها نه تنها در ارتباط با راه های هوایی کوچک هستند بلکه در بافت ریه هم دیده می شود. افزایش سلول های B در COPD در بیوبسی های برونشیال دیده می شود. لنفوئیدها شامل سلول های بالغ و حافظه ای بی سل یا تی سل می باشند. فولیکول های لنفوئیدی ثانوی شامل مرکزهای ژرمینال هستند و همچنین شامل سلول های بی سل – تی سل و دندرتیک سل و فولیکولار دندرتیک سل که موجب فعالیت بی و تی سل ها می شود هستند.در COPD فولیکول ها در ریه شاکل تجمع زیادی از بی سل ها هستند که توسط سی دی فور ها 80 تا 90 درصد و برخی از CD8 ها محاصره شده اند در این تجمع ها FDC وجود دارد که CD21 و CD35 می باشد.سلول های B عمدتا IGM مثبت هستند که نشان دهنده فعالیت آنها می باشند به علاوه مقدار زیادی از سلول های BCD27 هستند که در واقع سلول های حافظه ای هستند به علاوه سلول های CD138 هستند که پلاسما سل هستند و در این فولیکول ها وجود دارند. آنتی ژن های KI-67 در مرکز فولیکول ها دیده می شوند و لیگاند CD40 و خود CD40 هم در فولیکول ها یافت می شوند.
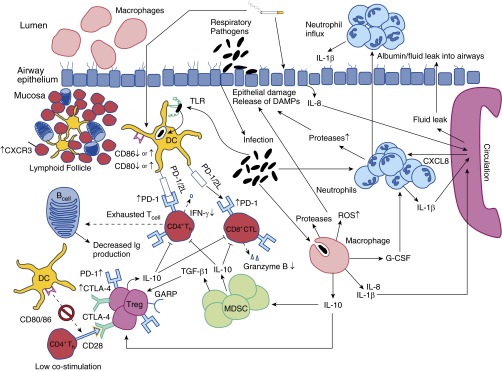
اکثر سلول های B در این فولیکول ها الیگوکولونال هستند از آنجایی که این فولیکول ها زیر پوشش راه های هوایی هستند به آنها بافت لنفوئیدی وابسته به برونکوس یا BALT گفته می شود. همچنین به این ساختمان ها ارگان های لنفوئیدی ترشیاری هم یا TLO می گویند.این ساختمان ها در واکنش به عفونت یا خود ایمنی ایجاد می شوند. گرچه هدف از این ساختمان ها از بین بردن عفونت می باشد ولی برخی از آنتی ژن ها قابل از بین بردن نیستن و در نتیجه التهاب مزمن ایجاد می شود.
در موش هایی که در معرض سیگار قرار می گیرند بعد از سه روز سلول های التهابی در ریه آنها مشاهده می شوند بین 3 تا 6 ماه بعد از شروع سیگار سلول های التهابی در لاواژ ریه آنها دیده می شود. فولیکول های لنفوئیدی بعد از 6 ماه پیدا می شوند و تعداد آنها با گذشت زمان افزایش پیدا می کند. بعضی از باکتری ها همانند هموفیلوس آنفولانزا که غیر دسته بندی هستند یا همان NTHI در راه های پایینی بیماری های بیماران COPD شدید دیده می شوند.
LPS یک محرک التهابی در باکتری های گرم منفی مانند NTHI می باشد.در موش هایی که در معرض LPS قرار گرفتن اطراف برونش ها و عروق های ریوی انتشار لنفوسیتی دیده می شوند. همچنین ویروس آنفولانزا هم می تواند موجب تشکیل این بافت های لنفوئیدی بشود. اینترلوکین IL-1β در ریه موش ها می تواند موجب التهاب ریه بزرگ شدن راه های هوایی کوچک فیبروز راه های هوایی و تجمع لنفوسیت ها در راه های هوایی بشود.اینترلوکین 6 موجب تجمع سلول های تک هسته ای در اطراف برونش ها و عروق ریوی می شوند. و باعث اکسپراسیون CXCL13 در بافت های لنفوئیدی می شوند که برای تشکیل این بافت ها ضروری هستند همچنین TNF-α موجب فیبروز و آنفیزم می شود.
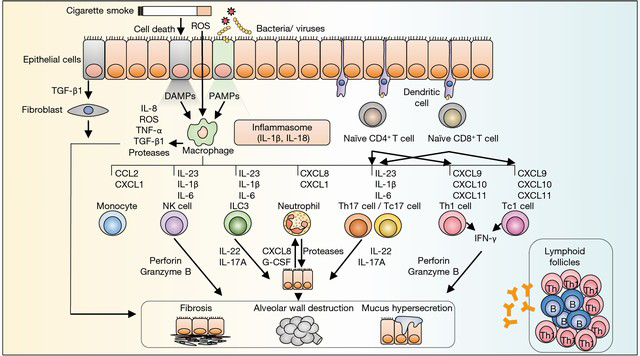
فولیکول های لنفوئیدی در بیماری های غیر از COPD هم مثل فیبروز ریه دیده می شود.همچنین در NSIP و برونشکتازی دیده می شود. LIP یک بیماری است که با انتشار وسیع سلول های بی و تی بالغ مشخص می شود. این انتشار در دیواره های آلوئولی دیده می شود. اما یک شکل با برونشیولیت فولیکولار قسمتی از این بیماری می باشد. توسعه فولیکول های لنفوئیدی با مراکز ژرمینال توسعه یافته یک شاخصه LIP می باشد در حال حاضر این بیماری قسمتی از بیماری های اتوایمون محسوب می شود. در بیماری برونشکتازی فولیکول ها اکثرا به صورت برونشیولیت فولیکولار هستند.
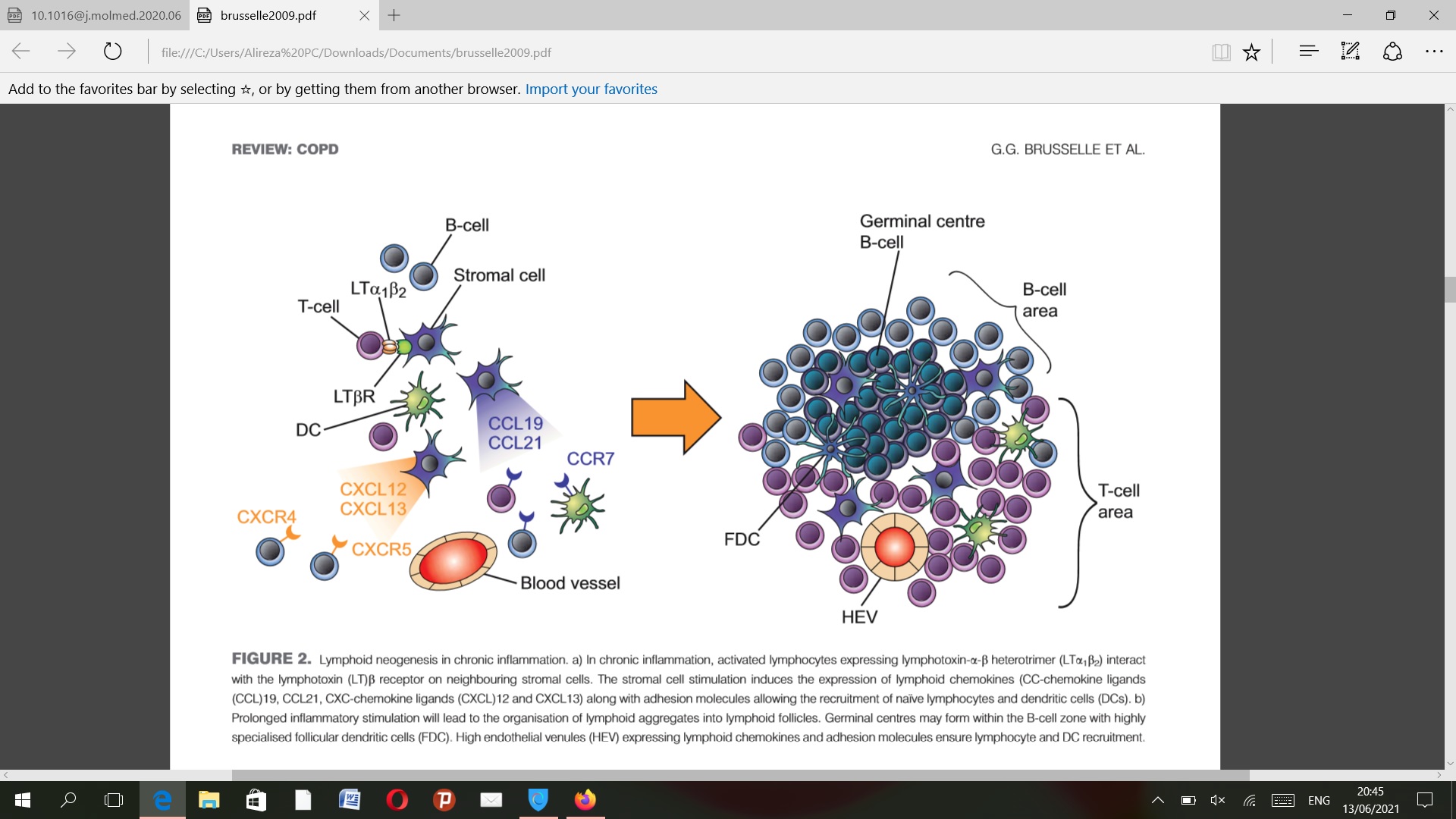
مکانیزم تشکیل فولیکول های لنفوئیدی نقش اصلی در تشکیل این فولیکول ها یک مولکولی است از خانواده TNF به نام LTα1β2 و رسپتور آن. در اتهاب مزمن لنفوسیت های فعال شده لنفوتوکسین LTα1β2 را اکسپرس می کنند که به رسپتور های روی سلول های استرومال می چسبد.در نتیجه سلول های استرومال تحریک می شوند و باعث ترشح کموکاین های لنفوئیدی شامل CCL19,21 و CXCL12,CXCL13 به اضافه مولکول های چسبنده می شوند و باعث جذب سلول های لنفوسیتی و دندرتیک می شود. CCL19,CCL21 باعث ارتشاح سلول های تی و دندرتیک می شود.CXCL12,CXCL13 که توسط دندرتیک های فولیکولار ترشح می شوند که به نوبه ی خود از سلول های استرومال مزانشیال نشئت می گیرند. و باعث ارتشاح سلول های بی در فولیکول ها می شود. فیبروبلاست ها هم باعث تشکیل ارگان های لنفوئیدی با تولید CXCL12 می شوند. سلول های دندرتیک سلول هایی هستند که در واقع APC هستند و زیر اپیتلیوم قرار دارند اخیرا این سلول ها از نوع لنگرین مثبت در اطراف راه های هوایی COPD به میزان زیادی دیده شده است. این سلول ها به نوبه ی خود باعث افزایش CCL20 می شود که این باعث تنظیم مهاجرت این سلول ها و ارتشاح سلول های تی سل می شود.
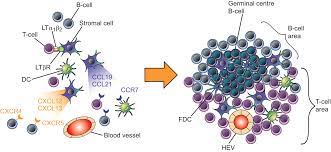
نقش فولیکول های لنفوئیدی بی سل ها می توانند تولید کننده IL4,6,13 و TNFα و لنفوتوکسین شوند. از آنجایی که در این فولیکول ها بی سل ها الیگوکولونال هستند آنها ممکن است در طی یک واکنش بومورال اختصاصی ایجاد شده باشند در حال حاضر 3 آنتی ژن محتمل است که موجب ارتشاح این سلول ها بشود
- در عفونت های مزمن باکتریایی و ویروسی در راه های هوایی کوچک افزایش سلول های لنفوسیتی دیده می شود بنابراین ممکن است ارتشاح سلول های بی و تی ممکن است در نتیجه واکنش به آنتی ژن های باکتریایی باشد. به همین دلیل این فولیکول ها در بیماری های COPD شدید و خیلی شدید دیده می شود. تقریبا در 52 درصد از بیماران COPD شدید با هموفیلوس آنفولانزا فونوموکوک PSA و موراسلا کاتارالیس کولونایز شده اند. تعداد حملات COPD با درجه وجود این باکتری ها در حالت استیبل وجود دارد. در حالی که وجود آنتی بادی ها بر علیه امکاتارالیس می تواند موجب از بین بردن این باکتری از بیماران COPD شود اما پاسخ آنتی بادی به PSA در 54 درصد از بیماران COPD با ناقل بودن مزمن این باکتری همراه است در نتیجه پاسخ آنتی بادی در مقابل این آنتی بادی نا موثر است.
- آنتی ژن های ناشی از تخریب مواد خارج سلولی می تواند درتشکیل دادن این فولیکول ها نقش داشته باشد.مثلا هیالورونیک اسید کلاژن و الاستین همه موجب ارتشاح نوتروفیل ها و منوسیدها می شوند. در نتیجه در بیماران آنفیزمی آنتی بادی های ضد الاستین وجود دارند که موجب ترشح و تولید بی سل ها می کنند.همچنین سیگار شامل حدود 4500 ماده مختلف می باشد. این مشتقات می توانند در مواد خارج سلولی ته نشین کنند و موجب ایجاد آنتی بادی شوند. گرچه وجود این فولیکول ها می تواند یک عامل بر ضد باکتری ها باشد اما ادامه پاسخ ایمنی در ریه به همراه تخریب بافت ریه موجب تحمل ایمنی می شود که این خود می تواند موجب عفونت های مزمن و التهاب مزمن شود. در بسیاری از بیماری های اتوایمن ما این فولیکول های لنفوئیدی را میبینیم.
آیا این فولیکول ها مفید هستند یا مضر . مثلا در مطالعه ای نشان داد که استفاده از ریتوکسی مب که باعث کاهش زیاد سلول های بی می شود باعث افزایش زیاد عفونت شده است.
اما برعکس اخیرا مشاهده شده است که در افراد سیگاری سلول های بی خاطره ای افزایش پیدا کرده است. اخیرا وجود آنتی بادی بر علیه سلول های اپیتلیال در بیماران COPD دیده شده است. بنابراین می توان تصور کرد که وجود چنین فولیکول هایی در عین حال می تواند مضر باشد.برای مثال در موش ها با تزریق آنتی بادی های ضد آندوتلیال توانسته اند آنفیزم ایجاد کنند.همچنین آنتی بادی های آنتی الاستین و آنتی اپیتلیال در بیماران COPD دیده می شود. در مطالعاتی تجمع IGG و C3 دیده شده است که ممکن است نقش این فولیکول ها را در ایجاد COPD ثابت بکند.
در بیمارانی که کورتن های حوراکی یا استنشاقی مصرف می کنند میزان این فولیکول ها در اطراف راه های هوایی کوچک کاهش پیدا کرده است. در نتیجه این مسئله در راه های هوایی کوچک احتمال افزایش عفونت دیده می شود.اما مکانیزم های متعددی وجود دارد که مفید بودن کورتن های استنشاقی را می تواند در بیماران COPD توجیه کند از جمله خصوصیت ضد التهابی کورتن های استنشاقی در کاهش سلول های التهابی شامل بی و سی در راه های هوایی و ریه می باشد. همچنین کورتن ها می توانند باعث تاثیر روی ایمنی ذاتی داشته باشند. همچنین کورتن ها باغث کاهش سیگنال های ناشی از سلول های اپیتلیال می شوند و باعث کاهش فعالیت سلول های دندرتیک می شوند.کورتن ها همچنین پاسخ سلول های بی و سی را کاهش می دهند. به خصوص با کاهش سایتوکاین های 4 و 5و 13( اینترلوکین ) .